Das Gesetz von Boyle-Mariotte
Das Gesetz von Boyle-Mariotte, auch Boyle-Mariottesches Gesetz oder Boyle-Mariotte-Gesetz und oft mit Boyle’sches Gesetz abgekürzt, sagt aus, dass der Druck idealer Gase bei gleichbleibender Temperatur und gleichbleibender Stoffmenge umgekehrt proportional zum Volumen ist. Erhöht man den Druck auf ein Gaspaket, wird durch den erhöhten Druck das Volumen verkleinert. Verringert man den Druck, so dehnt es sich aus.
Mathematisch wird das Boylesche Gesetz durch die Formel ausgedrückt:
(Näherungsformel ohne Berücksichtigung der Temperatur)
p • V = konstant
daraus folgt
p₁ • V₁ = p₂ • V₂
oder
p₁/p₂ = V₂/ V₁
mit
p₁: Anfangsdruck
V₁: Anfangsvolumen
p₂: Enddruck
V₂: Endvolumen
Wie sich dieser Effekt zur Umrechnung der Druckänderung bei einer Dichtheitsprüfung auf die Leckrate nutzen lässt erfahren Sie
Aus dem oben Genannten ergibt sich der Formelansatz zur Umrechnung Durchfluss / Druckänderung
(ohne Berücksichtigung der Temperatur):
pstart • Vstart = pend • Vend + pleck • Vleck
Da Vstart = Vend = VPrüfling + VSystem = VPrüf
und pleck = 1 bar (Umgebungsdruck), folgt:
VPrüf • (pstart – pend) = Vleck • 1 bar
⇒ Vleck = (VPrüf • Δp) / 1 bar
Normierung auf den Durchfluss (mit Prüfzeit):

oder umgestellt nach Δp:
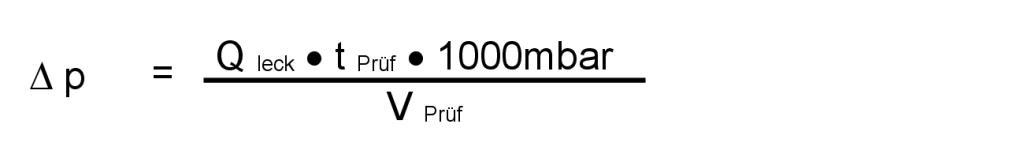
Kurz zusammengefasst, wie sich dieser Effekt zur Umrechnung der Druckänderung bei einer Dichtheitsprüfung auf die Leckrate nutzen ist es >hier<.


